LABORATORIO DE BIOLOGÍA DE TRYPANOSOMA CRUZI Y DE LA ENFERMEDAD DE CHAGAS
Responsable: Dra. Patricia Romano
En nuestro laboratorio estudiamos los mecanismos celulares y moleculares durante la infección de T. cruzi y las respuestas del hospedador, con el objeto de proponer mejoras tanto en el diagnóstico como en el tratamiento de la enfermedad de Chagas, una patología prevalente en América y con un creciente impacto a nivel mundial.
Líneas de investigación
1- Análisis del papel de las vías de transporte vesicular de la célula hospedadora durante la infección por T. cruzi en diferentes tipos de células, fagocitos profesionales y no profesionales
Investigamos el papel de proteínas que regulan el transporte vesicular en las vías endocítica, exocítica y autofágica (proteínas Rabs y SNAREs) en las distintas etapas de la infección por T. cruzi y la posible relación de las mismas con factores de virulencia parasitarios como cruzipaína.
Previamente describimos que la autofagia participa en el proceso de invasión de T. cruzi en fagocitos no profesionales y que la vacuola parasitófora adquiere la proteína autofagosomal LC3 en etapas tempranas de la infección (Romano et al, 2009; Romano et al, 2010), mientras que las proteínas SNARE VAMP7 y sus “partners” VTi1b y SNAP23 regulan la etapa de maduración de la vacuola en concordancia con la llegada de lisosomas (Cueto et al, 2017). Describimos también la participación de las proteínas Rab endocíticas (Rab 5, Rab21, Rab22 y Rab7) durante el transporte intracelular de la vacuola y su participación en el proceso global de infección (Salassa et al, 2020). De manera interesante Rab9 y Rab32 son reclutadas a la vacuola en forma específica, secuencial y con la participación, directa o indirecta, de cruzipaína, una cistepin proteasa parasitaria necesaria para el progreso de la infección, (Figura 1) (Salassa et al, 2024).
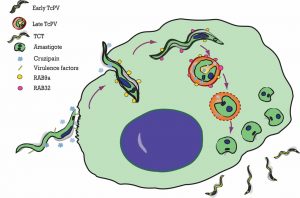
Figura 1: Rab 9 y Rab32 son reclutadas a la vacuola parasitófora de T. cruzi de forma secuencial. Este fenómeno es regulado por factores de virulencia parasitarios como cruzipaína.
2- Estudio del rol de la autofagia en el transcurso de la infección por T. cruzi en ratones y de su función moduladora de la respuesta inmune.
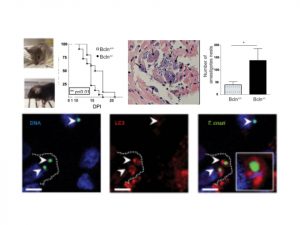
Previamente demostramos que la deficiencia autofágica, en ratones genéticamente modificados (ratones “knock out” heterocigotas para la proteína autofágica Beclina-1), produce una infección más agresiva elevando los valores de parasitemia y parasitismo cardíaco, produciendo la muerte temprana de estos ratones (Casassa et al, 2019). Recientemente demostramos que la inducción de la autofagia por Ácido Ursólico favorece la eliminación de amastigotes en los macrófagos infectados y en otros tipos celulares por el proceso de Xenofagia (Vanrell et al, 2022) por lo que continuamos estudiando la participación de la autofagia en el desarollo de las respuestas inmunes innata y adaptativa que se activan durante la infección por T. cruzi (Aguilera et al, 2024).
Figura 2: ratones “knock out” heterocigotas para Beclina-1 (Bcl-1-/-), con menor actividad autofágica, presentan menor supervivencia y mayor parasitismo cardíaco. Macrófagos peritoneales provenientes de ratones “wild type” rodean los amastigotes intracelulares con membranas LC3 positivas (xenofagia).
3- Estudio del rol de factores de virulencia de T. cruzi en el ciclo biológico examinando principalmente la infección y diferenciación parasitaria.
En nuestro laboratorio hemos caracterizado el funcionamiento de la vía autofágica de T. cruzi durante la diferenciación parasitaria que ocurre tanto en el insecto vector como en la célula humana. Por medio del uso de drogas específicas, hemos demostrado que la regulación de esta vía en T. cruzi presenta similitudes y diferencias con la regulación de la misma en las células de mamíferos siendo las diferencias un foco interesante de estudio en la búsqueda de posibles blancos terapéuticos (Vanrell et al, 2017). Además encontramos que la autofagia parasitaria regula la actividad de cruzipaína, uno de los principales factores de virulencia parasitarios (Losinno et al, 2021). De manera interesante, observamos que cruzipaína se halla en las vesículas extracelulares secretadas por T. cruzi durante la diferenciación de tripomastigotes a amastigotes y que su inhibición reduce el reclutamiento de Rab9 y Rab32 a la vacuola parasitófora (Salassa et al, 2024) permitiendo postular que este factor parasitario sería clave para favorecer la infección.
4- Análisis del efecto de drogas que afectan el desarrollo de la infección por T. cruzi, con blancos en el parásito o en el hospedador y que puedan ser utilizadas para el tratamiento de la Enfermedad de Chagas.
A partir de los datos obtenidos de la investigación básica, estudiamos el efecto de compuestos, naturales o sintéticos, que pueden inhibir blancos específicos en el parásito o en el hospedador afectando el desarrollo normal de la infección por T. cruzi, como en el caso del Ácido ursólico (Vanrell eta al, 2022. Una estrategia es usar drogas de reposicionamiento, es decir compuestos ya aprobados para su uso en otras patologías y que puedan ser utilizados para una nueva indicación considerando una dosis efectiva y terapéuticamente segura. Hemos encontrado que carvedilol, un compuesto ampliamente usado para el tratamiento de la hipertensión arterial, inhibe la autofagia parasitaria y reduce significativamente la infección (Rivero et al, 2021). Actualmente estamos analizando las dosis y regímenes terapéuticos de este compuesto tanto en modelos de infección in vitro como in vivo en ratones como una nueva propuesta terapéutica para el tratamiento de la enfermedad de Chagas.